Jak wysłać chorobotwórcze białko na „molekularny śmietnik”?
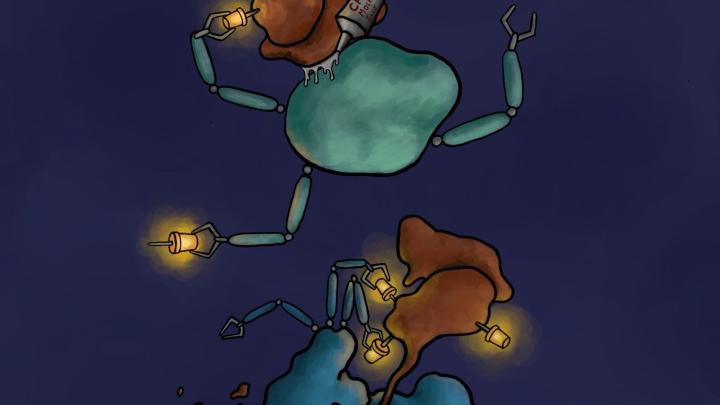
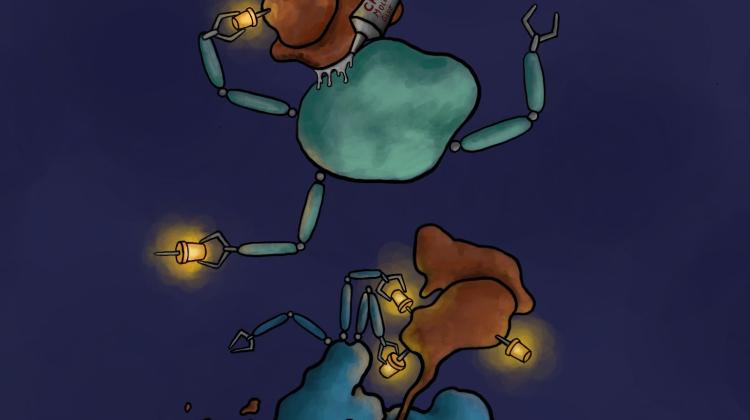 Rysunek przedstawia mechanizm działania degradera - kleju molekularnego. Degrader CR8 powoduje sklejenie kompleksu cykliny K/CDK12 (kolor brązowy) z ligazą ubikwitynowa (kolor zielony), co prowadzi do ubikwitynacji cykliny K (żółte pinezki). Powoduje to degradację cykliny K przez proteozom, czyli "molekularny śmietnik" (kolor niebieski). Autor: Jonas Koeppel.
Rysunek przedstawia mechanizm działania degradera - kleju molekularnego. Degrader CR8 powoduje sklejenie kompleksu cykliny K/CDK12 (kolor brązowy) z ligazą ubikwitynowa (kolor zielony), co prowadzi do ubikwitynacji cykliny K (żółte pinezki). Powoduje to degradację cykliny K przez proteozom, czyli "molekularny śmietnik" (kolor niebieski). Autor: Jonas Koeppel.
Związek działający jak klej łączący źle działające białko z innym białkiem, które je unieszkodliwia, odprowadzając na nasz komórkowy "molekularny śmietnik" znaleźli m.in. polscy naukowcy. To krok na drodze do identyfikacji kolejnych klejów molekularnych, mających zastosowanie np. w celowanej terapii nowotworowej.
Kiedy w organizmie jakieś białko nie działa tak, jak powinno, może to wywołać chorobę, np. nowotwór. Leki wykorzystywane w leczeniu różnych stanów chorobowych oddziałują zwykle na wybrane patogenne białka. Kleje molekularne to nowatorski mechanizm działania leków, który umożliwia unieszkodliwienie nawet tych białek, które do tej pory znajdowały się poza zasięgiem farmakologii.
W rozmowie z PAP, swoje odkrycie nowego rodzaju „kleju molekularnego” komentuje dwójka polskich naukowców, Zuzanna Kozicka z Friedrich Miescher Institute for Biomedical Research w Bazylei i Mikołaj Słabicki z Broad Institute of MIT and Harvard w Cambridge, Dana-Farber Cancer Institute w Bostonie, USA i Niemieckiego Centrum Badań nad Rakiem w Heidelbergu.
„Białka to podstawowy materiał, z którego są zbudowane nasze komórki i który zapewnia im prawidłowy rozwój. Problem pojawia się wtedy, gdy takie białko się popsuje i zainicjuje niekontrolowany podział komórki, co może zapoczątkować rozwój choroby nowotworowej” – mówi Mikołaj Słabicki.
"Ważną grupą białek są enzymy, które kierują wszystkimi zmianami chemicznymi w komórce. Najważniejszy fragment enzymu to miejsce aktywne, które odpowiada za działanie danego białka. Zazwyczaj opracowując potencjalny lek, szukamy związku chemicznego, który będzie idealnie pasował do kształtu miejsca aktywnego białka, które chcemy zahamować - tak jak dopasowuje się klucz do zamka w drzwiach. Taki klucz może zatrzymać działanie rozregulowanego, chorobotwórczego białka” – tłumaczy Zuzanna Kozicka.
Ale problem polega na tym, że nie wszystkie białka mają takie miejsca aktywne. „Gdy chcemy unieszkodliwić źle działające białko to często po prostu nie mamy szans na znalezienie odpowiedniego klucza – a wiele takich białek odgrywa ważną rolę w rozwoju nowotworów. Dlatego bardzo potrzebne są innowacyjne podejścia, które umożliwią nam opracowanie leków działających w nowy sposób" – dodaje Kozicka.
Jeden z pomysłów to tzw. celowana degradacja białek. Polega ona na przechytrzeniu komórki i zmuszeniu jej do zniszczenia chorobotwórczego białka przy wykorzystaniu istniejącej w każdej komórce „maszynerii molekularnej” odpowiedzialnej za pozbywanie się zbędnych lub nieprawidłowych białek (układ ubikwityna – proteasom). Aby białko zostało zniszczone, musi najpierw zostać oznaczone za pomocą specjalnego drobnocząsteczkowego białka, ubikwityny, przez enzym wspomnianej „maszynerii molekularnej” zwany ligazą ubikwitynową. Celowaną degradację niepożądanego białka można więc osiągnąć przy użyciu „kleju molekularnego” łączącego dane białko z ligazą.
Mikołaj Słabicki, Zuzanna Kozicka i Georg Petzold stanowią trzon międzynarodowego zespołu naukowców, który pod kierownictwem prof. Benjamina Eberta z Dana-Farber Cancer Institute i dr Nicolasa Thomä z Friedrich Miescher Institute for Biomedical Research, szukał związków, które powodowałyby degradację białek. Wyniki swoich poszukiwań naukowcy opublikowali w prestiżowym czasopiśmie „Nature” https://rdcu.be/b4BiT.
Korzystając z ogromnych baz danych, badacze znaleźli związek CR8 działający jako klej molekularny wymuszający oznakowanie ubikwityną, a co za tym idzie – zniszczenie białka odpowiedzialnego za rozwój choroby. Naukowcy analizowali, jak po podaniu CR8 do komórki zmienia się ilość wszystkich białek w komórce. Okazało się, że ilość wszystkich białek pozostawała niezmieniona, oprócz jednego: cykliny K. Kolejne eksperymenty potwierdziły, że właśnie to białko, które prawdopodobnie przyczynia się do rozwoju nowotworów, ląduje na „molekularnym śmietniku”, poprzez wymuszone przez CR8 sklejenie go z jedną z ligaz ubikwitynowych.
Jak tłumaczy Zuzanna Kozicka, w takiej sytuacji zamiast inhibitora, czyli kluczyka wkładanego w miejsce aktywne, mamy tzw. degrader - cząsteczkę, które pozwala nam precyzyjnie naznaczyć niepożądane, źle działające białko i spowodować jego degradację w komórce. To otwiera możliwości dezaktywowania takich źle funkcjonujących białek, których do tej pory nie mogliśmy unieszkodliwić, bo na przykład nie mają one miejsc aktywnych albo nie posiadają stabilnej struktury przestrzennej.
Badacze rozwiązali też strukturę krystaliczną pozwalającą im zobrazować sklejone przez CR8 białka. "Rozszyfrowanie jak łączą się ze sobą te poszczególne części układanki pozwala nam lepiej zrozumieć działanie klejów molekularnych. Pozwala też powoli zacząć myśleć o tzw. ‘racjonalnym projektowaniu’ tego typu leków, czyli wymyślaniu, jak powinien wyglądać związek chemiczny, który połączyłby ze sobą dwa wybrane białka – choć nadal jest to bardzo trudne zadanie" – komentuje Zuzanna Kozicka.
Mikołaj Słabicki dodaje, że do tej pory znane były tylko dwie grupy związków określanych jako kleje molekularne, a wiele firm farmaceutycznych inwestuje obecnie w tego rodzaju badania, bo dzięki takim związkom można będzie leczyć choroby, na które nie było dotąd skutecznych i bezpiecznych lekarstw: "Pokazaliśmy, że takich związków jest więcej, że trzeba i warto ich szukać".
PAP - Nauka w Polsce, Ewelina Krajczyńska
ekr/ agt/
Przed dodaniem komentarza prosimy o zapoznanie z Regulaminem forum serwisu Nauka w Polsce.